Жидкость в плевральной полости при циррозе печени и сердечной недостаточности возникает в результате затрудненного обмена жидкости в организме. При циррозе печени нарушается синтез альбуминов, что ведет к снижению онкотического давления и повышению проницаемости сосудов, что способствует накоплению жидкости в плевральной полости. В свою очередь, сердечная недостаточность приводит к застойному явлению, увеличивая венозное давление и способствуя отеку тканей.
В обоих случаях скопление жидкости может привести к развитию плеврита и ухудшению дыхательной функции. Поэтому важно раннее выявление и лечение этих состояний, направленные на коррекцию основного заболевания и уменьшение количества жидкости в плевральной полости.
- Определение: Жидкость в плевральной полости (плевральный выпот) является общим осложнением цирроза печени и сердечной недостаточности.
- Механизмы возникновения: При циррозе печени выпот возникает из-за увеличенного давления в воротной вене и нарушения белкового обмена, при сердечной недостаточности — из-за застоя крови и повышения гидростатического давления в легочных капиллярах.
- Клинические проявления: Симптомы могут включать одышку, кашель, боль в груди и уменьшение физической активности.
- Диагностика: Для выявления плеврального выпота используются рентгенография грудной клетки, ультразвуковое исследование и анализ плевральной жидкости.
- Лечение: Терапия зависит от основной причины: управление циррозом или сердечной недостаточностью, диуретики, удаление жидкости (плевроцентез).
- Прогноз: Прогноз зависит от основной болезни и тяжести состояния пациента; лечение основного заболевания может улучшить симптоматику.
Жидкость в плевральной полости при циррозе печени и сердечной недостаточности
Егай А.А., Бебезов Б.Х., Казакбаев А.Т., Двумаров А.А., Тентимишев А.Э.
Фейгин А.М., Суров Э.А.
1 Кыргызско-Российский Славянский университет им. Б.Н. Ельцина, 2 Национальный госпиталь при министерстве здравоохранения Кыргызской Республики
Печеночный гидроторакс – это плевральный выпот у пациентов с циррозом печени и портальной гипертензией в отсутствие заболеваний сердца и легких. До сих пор образование печеночного гидроторакса до конца не изучено, наиболее приемлемое объяснение – это прямое попадание асцитической жидкости в плевральную полость через дефекты в диафрагме на фоне повышения давления в брюшной полости и под действием присасывающей силы негативного давления в плевральной полости.
Клинический ход печёночного гидроторакса может проявляться как без симптомов, так и с одышкой, сухим кашлем и болевыми ощущениями. В некоторых случаях коррекция плеврального выпота с использованием медикаментозной терапии, питьевого режима, снижения потребления соли и торакоцентеза оказывается неэффективной, что свидетельствует о наличии рефрактерного потока.
В таких ситуациях возникает необходимость в постоянных процедурах торакоцентеза, что увеличивает риск различного рода осложнений. В рамках данной статьи отображены результаты применения химического плевродеза с йодповидоном в качестве паллиативной терапии для данной категории больных. Описаны ключевые моменты индукции плевродеза при наличии асцита, а также проведена оценка не только его эффективности, но и безопасности использования йодповидона.
При циррозе печени накопление жидкости в плевральной полости является довольно распространенным клиническим симптомом. Это связано с развивающейся портальной гипертензией, которая ведет к нарушению венозного оттока и увеличению давления в системе воротной вены. В результате этого нарушается баланс между артериальной и венозной системами, что способствует выходу жидкостей в плевральное пространство. Кроме того, синтез альбумина в печени снижается, что приводит к уменьшению онкотического давления и усиливает отечность.
Сердечная недостаточность также играет важную роль в патогенезе плеврального выпота. Из-за ухудшения насосной функции сердца, наблюдаются застойные явления в легочных венах, что может приводить к отеку легочной ткани и выходу жидкости в плевральную полость. Миокард может не обеспечивать надлежащий уровень сердечного выброса, что также увеличивает системное и местное давление в венозной системе. Чаще всего это наблюдается при левожелудочковой недостаточности, где застоявшаяся кровь напрямую влияет на легочные сосуды.
В клинической практике важно учитывать, что наличие жидкости в плевральной полости у пациентов с циррозом печени и сердечно-сосудистыми заболеваниями требует комплексного подхода к диагностике и лечению. Это могут быть как консервативные методы, такие как диуретическая терапия, так и инвазивные процедуры, например, дренирование плевральной полости. Учитывая взаимосвязь между этими состояниями, необходимо тщательно следить за состоянием пациентов, предотвращая возможные осложнения и улучшая качество жизни.

488 KBцирроз печенипеченочный гидротораксасцитплевродезйодповидон
1. Arroyo V., Ginès P., Gerbes A.L., Dudley F.J., Gentilini P., Laffi, G., Reynolds T.B., Ring-Larsen H., Schölmerich J. Определение и диагностические критерии рефрактерного асцита и гепаторенального синдрома при циррозе. International Ascites Club. Hepatology (Baltimore, Md.). 1996. Т. 23. № 1. С. 164–176. DOI: 10.1002/hep.510230122.
2. Machicao V.I., Balakrishnan M., Fallon M.B. Респираторные осложнения при хронических заболеваниях печени. Hepatology. 2014. Т.
59. № 4. P. 1627–1637.
DOI: 10.1002/hep.26745.
3. Singh A., Bajwa A., Shujaat A. Обзор по управлению печёночным гидротораксом, основанный на доказательствах. Respiration. 2013. Т. 86. № 2. С. 155–173.
DOI: 10.1159/000346996.
4. Runyon B.A., AASLD Practice Guidelines Committee. Management of adult patients with ascites due to cirrhosis: an update. Hepatology (Baltimore, Md.). 2009. Vol.
49. № 6. Р. 2087–2107.
DOI: 10.1002/hep.22853.
5. Chen A., Massoni J., Jung D., Crippin, J. Установление дренажных туннелированных катетеров для управления печёночным гидротораксом. Пилотное исследование. Annals of the American Thoracic Society. 2016. Т.
13. № 6. P. 862–866.
DOI: 10.1513/AnnalsATS.201510-688BC.
6. Bernardi M., Moreau R., Angeli P., Schnabl B., Arroyo V. Mechanisms of decompensation and organ failure in cirrhosis: from peripheral arterial vasodilation to systemic inflammation hypothesis. Journal of hepatology. 2015. Vol. 63. № 5. P. 1272–1284.
DOI: 10.1016/j.jhep.2015.07.004.
7. Norvell J.P., Spivey J.R. Печёночный гидроторакс. Clinics in liver disease. 2014. Т.
18. № 2. P. 439–449.
DOI: 10.1016/j.cld.2014.01.005.
8. Huang P.M., Kuo S.W., Chen J.S., Lee J.M. Thoracoscopic mesh repair of diaphragmatic defects in hepatic hydrothorax: a 10-year experience. The annals of thoracic surgery. 2016. Vol.
101. № 5. P. 1921–1927. DOI: 10.1016/j.athoracsur.2015.11.023.
9. Kim J.S., Kim C.W., Nam H.S., Cho J.H., Ryu J.S., Lee H.L. Печёночный гидроторакс без асцита как первый признак цирроза печени. Respirology case reports. 2015. Т.
4. № 1. Р. 16–18. DOI: 10.1002/rcr2.140.
10. Ivashkin V.T., Mayevskaya M.V., Pavlov C.S., Fedosyina Y.A., Bessonova Y.N., Pirogova I.Y., Garbuzenko D.V. Лечение осложнений цирроза печени: Клинические рекомендации Российской научной ассоциации по печени и Российской гастроэнтерологической ассоциации. Рос Журнал Гастроэнтерол, Гепатол, Колопроктол. 2016. Т.
26. № 4. P. 71–102. DOI: 10.22416/1382-4376-2016-26-4-71-102.
11. Solà E., Solé C., Ginès P. Management of uninfected and infected ascites in cirrhosis. Liver international: official journal of the International Association for the Study of the Liver. 2016. Vol. 36.
No. 1. С. 109–115. DOI: 10.1111/liv.13015.
12. Lv Y., Han G., Fan D. Hepatic Hydrothorax. Annals of hepatology. 2018. Vol. 17. № 1. Р. 33–46.
DOI: 10.5604/01.3001.0010.7533.
13. Orman E.S., Lok. A.S. Outcomes of patients with chest tube insertion for hepatic hydrothorax.Hepatology international. 2009. Vol.
3. No.
4. С. 582–586.
DOI: 10.1007/s12072-009-9136-z.
14. Suarez P.M., Gilart J.L. Плевродез в лечении пневмоторакса и плеврального выпота. Monaldi Arch Chest Dis. 2013. Т.
79.
No. 2. P. 81–86.
15. Jung Y. Хирургическое лечение печёчного гидроторакса: «Четырехступенчатый подход». The Annals of thoracic surgery. 2016. Т. 101.
No.
3. P. 1195–1197. DOI: 10.1016/j.athoracsur.2015.04.110
Патологическое накопление жидкости в плевральной полости, называемое гидротораксом, может быть одним из осложнений декомпенсированного цирроза печени (ЦП). Одним из наиболее первых, клинически значимых, осложнений ЦП является асцит, примерно в 10–20 % асцит не поддается медикаментозной коррекции [1].
Печеночный гидроторакс (ПГ) – это скопление плевральной жидкости в объеме, превышающем 500 мл у пациентов с ЦП, при этом исключено наличие сопутствующей патологии сердца и легких [2]. ПГ встречается реже, чем асцит, примерно, у 15 % пациентов с циррозом и в 25 % случаев течение гидроторакса рефрактерно к консервативному лечению [3].
Даже минимальное количество гидроторакса может привести к проявлениям дыхательной недостаточности. Когда стандартная терапия асцита и ПГ оказывается неэффективной, возникает необходимость в хирургических вмешательствах для удаления жидкости (парацентез, торакоцентез). Эти процедуры налагают значительное бремя как на пациентов, так и на здравоохранительную систему. В соответствии с рекомендациями Американской ассоциации по изучению заболеваний печени 2009 года, установка дренажа в брюшной и плевральной полостях считается противопоказанной, так как данная процедура существенно повышает риск летальности [4]. Однако эти рекомендации были сделаны без исчерпывающего описания типов дренажного оборудования и целевой установки манипуляций.
В 2016 г. произведено исследование, в котором были получены положительные результаты катетеризации плевральной полости у пациентов с ЦП, которые были кандидатами на трансплантацию печени [5]. В статье приводилось наблюдение 24 пациентов, из них у 4 (16,7 %) возникло инфицирование плевральной полости, трем из которых это не помешало успешно произвести трансплантацию печени [5]. У 8 пациентов (33,3 %) имел место спонтанный плевродез, что позволило удалить дренаж из грудной полости [5].
Ключевым патогенетическим механизмом, ведущим к образованию асцита, является портальная гипертензия. Печень выполняет роль единственного органа, который вырабатывает альбумин, и, следовательно, её повреждение приводит к гипоальбуминемии и, как следствие, к снижению онкотического давления, что и обуславливает образование асцита.
В последнее время общепринятой является гипотеза периферической артериальной вазодилятации [6]. Портальная гипертензия увеличивает поступление вазодилятаторов в кровяное русло, что постепенно ведет к застою крови в сосудах органов брюшной полости. Данное состояние вызвано активацией симпатической нервной системой, ренин-ангиотензин-альдостероновой системы, секрецией вазопрессина, что ведет к задержке натрия и выходу жидкости во внесосудистое пространство, в частности в брюшную полость [6]. Другим источником вазодилятаторов может быть кишечник, когда продукты жизнедеятельности бактерий стимулируют высвобождение провоспалительных цитокинов, что ведет к расширению сосудов органов брюшной полости [6].
Причина образования ПГ при ЦП описана несколькими теориями, в том числе нарушение пластической функции печени и, как следствие, снижение онкотического давления за счет гипоальбуминемии, повышение гидростатического давления в системе непарной вены, трансдиафрагмальная миграция асцитической жидкости в плевральную полость [7]. Несмотря на это, наиболее общепринятой является теория поступления жидкости из брюшной полости через дефекты в диафрагме. Данные дефекты диафрагмы были описаны и классифицированы P.M. Huang et al., который также предложил торакоскопическое закрытие дефектов сеткой [8]. Данная теория также не противоречит изолированному ПГ, так как при этом скорость реабсорбции асцита плевральной полостью равна образованию асцита брюшной полостью [9].
Пункция плевральной полости проводится для пациентов с ПГ, которые не реагируют на консервативную терапию, а также при наличии клинических признаков плеврального выпота, таких как одышка и сухой кашель. В условиях декомпенсации ЦП эффект от торакоцентеза, как правило, кратковременен, что вызывает необходимость в повторных процедурах.
Эвакуация плевральной жидкости, в свою очередь, ведет к потере белка и электролитов. Стоит упомянуть, что сам торакоцентез несет в себе такие осложнения, как пневмоторакс, кровотечение, инфицирование плевральной полости, повреждение печени и селезенки, болевой шок и отек лёгкого, вероятность которых возрастает с каждой повторной процедурой [12].
К дренированию плевральной полости необходимо подходить с крайней осторожностью, так как существует риск таких осложнений, как обильная потеря белка, вторичная инфекция, пневмоторакс, гемоторакс, печеночно-почечный синдром, нарушение электролитного баланса [13]. Традиционно считалось, что показаниями к дренированию плевральной полости являются эмпиема плевры и пневмоторакс.
Сейчас данная процедура стала общепринятой в лечении пациентов с рецидивными и рефрактерными плевральными выпотами, при этом затяжное нахождение трубки в грудной полости удается прервать индукцией плевродеза. Химический или медикаментозный плевродез – это искусственная инициация асептического воспаления париетального и висцерального листка плевры путем введения местнораздражающего вещества. В результате чего происходит нивелирование плевральной полости и, как следствие, такие состояния, как плевральный выпот и пневмоторакс, не имеют место быть. Плевросклерозант вводится в плевральную полость либо через дренаж, либо во время лечебно-диагностической плевроскопии или торакоскопии. Наиболее распространенными химическими веществами являются тальк, тетрациклин и его производные, йодповидон, нитрат серебра, цитостатические препараты [14].
Цель исследования: оценить эффективность применения ХП йодповидоном у пациентов с рефрактерным плевральным выпотом при ЦП в сочетании с таким осложнением, как асцит. На основании показателей гемодинамики, температурной и болевой реакции установить, безопасен ли данный метод плевродеза. Отметить особенности проведения плевродеза при сочетанном наличии асцита и плеврального выпота.
Исследование проводилось на базе клиники имени И.К. Ахунбаева Национального госпиталя при Министерстве здравоохранения Кыргызской Республики. Стоит отметить, что в данном медицинском учреждении располагается ведущее отделение торакальной хирургии республики.
В период с сентября 2019 года по октябрь 2021 года в стационаре лечилось 12 пациентов с циррозом печени различной этиологии в возрасте от 41 до 67 лет, среди которых 6 мужчин (50 %) и 6 женщин (50 %). Все больные находились под постоянным наблюдением гастроэнтеролога и периодически проходили коррекцию лечения в стационаре. Однако у всех пациентов развились осложнения, включающие портальную гипертензию, асцит и гидроторакс. Правосторонний гидроторакс был выявлен у всех 12 участников, из которых в 3 случаях (25 %) было зарегистрировано наличие небольшого выпота в левой плевральной полости.
В стадии декомпенсации ЦП, невзирая на коррекцию медикаментозного лечения, у пациентов развивалась клиника дыхательной недостаточности, с целью ее купирования проводились процедуры торакоцентеза, больные, у кого течение ПГ носило рецидивный и рефрактерный характер, были госпитализированы в отделение торакальной хирургии для проведения процедуры ХП. Учитывая, что ранее индукция плевродеза не проводилась и данный способ лечения не входит в протоколы Министерства здравоохранения Кыргызской Республики, у всех пациентов было взято информированное согласие.
В исследование не были включены пациенты с аллергическим анамнезом к препаратам йода, заболеваниями щитовидной железы, ригидным легким и пациенты с ожидаемой продолжительностью жизни менее 30 дней.
Методика химического плевродеза включала дренирование плевральной полости, анестезию плевральных листков, а сама процедура плевродеза осуществлялась лишь после полной разбухания легкого, что подтверждалось рентгенографией. Местная анестезия достигалась через введение 50 мл 1 % раствора лидокаина в плевральный дренаж, экспозиция составляла 20 минут. Затем анестетик удалялся из полости, и внутриплевременно вводилось 20 мл 10 % раствора йодповидона, дренаж закрывался на 2 часа; для достижения наибольшего эффекта больным рекомендовалось менять позу тела и выполнять дыхательные упражнения.
Оценка эффективности заключалась в уменьшении количества отделяемого по дренажу до 100 мл и, как следствие, возможности удаления дренажа из плевральной полости. Пациенты после выписки находились на амбулаторном наблюдении торакального хирурга, контрольные осмотры проводились через 1, 3 и 6 месяцев, далее раз в год. Безопасность процедуры контролировалась путем фиксации основных показателей гемодинамики, температурной реакции и болевых ощущений.
Результаты исследования и их обсуждение
Статистическая обработка данных проводилась с помощью программы IBM Statistics 28.0.
Причиной ЦП в 11 случаях (91,7 %) стал хронический вирусный гепатит, в 1 случае (8,3 %) причиной стал первичный билиарный цирроз печени. У 9 пациентов (75 %) на момент обращения имел место субтотальный уровень жидкости, у 2 пациентов (16,7 %) правый гемоторакс был затенен полностью, у 1 пациента (8,3 %) на рентгенографии обнаружен гидропневмоторакс с тотальным коллапсом правого легкого (рисунок), что, вероятнее, стало осложнением многочисленных пункций плевральной полости. С целью предупреждения смещения средостения эвакуация жидкости из грудной полости производилась поэтапно, объем жидкости за первые сутки составил от 2800 мл до 4100 мл. Ежесуточный объем отделяемой жидкости составил от 350 до 1400 мл. У всех пациентов диагностировано наличие асцита различной степени тяжести: умеренный асцит в 9 случаях (75 %) и в 3 случаях (25 %) имел место асцит тяжелой степени.
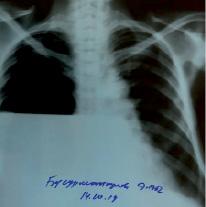
Правосторонний гидропневмоторакс. Рентгенограмма в прямой проекции демонстрирует горизонтальный уровень жидкости с верхней границей на уровне переднего края III ребра.
В 6 случаях (50 %) ХП был произведен без предварительной эвакуации жидкости из брюшной полости. Таким образом, не был достигнут минимальный объем ежедневной экссудации в 100 мл, который мог бы позволить удалить дренаж из плевральной полости. Все 6 пациентов были выписаны на амбулаторное наблюдение и лечение с дренажными трубками из плевральной полости.
Данная группа пациентов начала стационарное лечение в торакальном отделении раньше. Отсутствие успеха химической плевродезы можно объяснить постоянной миграцией асцитической жидкости в плевру и изменениями концентрации активного вещества. В ходе амбулаторного наблюдения у 2 пациентов (33,3 %) произошло прекращение поступления жидкости в течение 12 и 14 дней без рецидивов, в то время как у 4 пациентов (66,7 %) из-за длительного нахождения дренажной трубки развилась плевральная эмпиема, что в 3 случаях привело к облитерации плевры в течение месяца, а в одном случае — к рецидиву эмпиемы через 3 месяца после удаления дренажа. Результаты эффективности химической плевродезы представлены в таблице 1.
Сравнение эффективности ХП у пациентов с ЦП без лапароцентеза и с лапароцентезом (p < 0,05)
Количество дней до удаления дренажа после ХП
При каких заболеваниях появляется плевральный выпот
- Травма, коагулопатия, разрыв аорты или легочной артерии могут привести к гемотораксу — скоплению крови в плевральной полости;
- Эмпиема плевры, связанная с пневмонией, абсцессами легкого или печени, инфекциями после травм или торакотомии, может вызывать пиоторакс;
- Повреждения лимфатических сосудов в результате травм, прорастание опухолей или синдром верхней полой вены приводят к хилотораксу — скоплению лимфы, содержащей триглицериды;
- Сердечная недостаточность — в 80% случаев вызывает двусторонний плевральный выпот;
- Цирроз печени с асцитом — асцитическая жидкость может просачиваться в плевральную полость через дефекты диафрагмы, в 70% случаев у пациентов развивается правосторонний выпот;
- Заболевания почек, такие как нефротический синдром и гломерулонефрит;
- Гипоальбуминемия, сопровождающаяся отеками и анасаркой, в 90% случаев приводит к двустороннему выпоту;
- Перикардит в сочетании с анасаркой и асцитом;
- Онкологические заболевания, чаще всего рак молочной железы, легких, яичников, лимфома, саркоидоз, метастазы в плевру;
- Тромбоэмболия;
- Вирусные инфекции, включая ВИЧ;
- Аутоиммунные заболевания: ревматоидный артрит, системная красная волчанка, гипотиреоз и др.
В некоторых случаях данные патологии выявляются случайно во время обследования. Однако чаще наблюдаются различные симптомы, наиболее характерные из которых:
- Одышка — это наиболее распространённый симптом плеврального выпота, который первоначально возникает при физической нагрузке и с увеличением объёма жидкости становится более выраженным;
- Ощущение боли в области груди, усиливающееся при вдохе, кашле или смехе, может иррадиировать в шею, плечо или живот. У пациента возможно появление давления и тяжести в груди, что становится более выраженным во время физической активности; для облегчения состояния, особенно при синдроме плеврального выпота, человек принимает вынужденное положение.
- Ирритированная плевра может вызвать появление сухого, чаще всего мучительного кашля.
- Непрерывная потеря белков и электролитов с экссудатом может привести к истощению организма пациента.
В зависимости от причины патологии болезненные ощущения могут быть на стороне поражения, например, при пневмонии, туберкулезе и т.д., или двусторонними, что характерно, например, при сердечной недостаточности, заболеваниях почек и др. При появлении правостороннего или левостороннего плеврального выпота грудная клетка движется неравномерно, пораженная сторона запаздывает на вдохе.
Поскольку выпот — проявление различных заболеваний, клиническая картина дополняется целым рядом других признаков. Так, при выпоте в плевральной полости при онкологии возможно слабость, повышение температуры, утомляемость, резкая потеря веса и др., при гипоальбуминемии — отечность лица, конечностей, при патологиях печени — асцит, сердца — анасарка и т. д.
Лечение
Для эвакуации выпота проводится дренирование плевральной полости с помощью пункции или торакоцентеза, после чего состояние пациента улучшается. Как правило, дренаж, соединенный со специальным резервуаром, устанавливается в плевральную полость на определенное время — для постепенного выведения скапливающейся жидкости. При частых рецидивах, при отсутствии эффекта от дренирования рекомендовано проведение плевродеза — в ходе процедуры в плевру вводится склерозирующее вещество, что приводит к облитерации плевральных листков, и появление между ними выпота в дальнейшем становится невозможным.
Также необходимо назначение препаратов, действие которых направлено на лечение основного заболевания: антибиотиков, цитостатиков, противирусных, противовоспалительных средств и др. В качестве вспомогательного лечения при выпоте в плевральной полости показана оксигенотерапия, диета с ограничением соли, физиотерапевтическое лечение.
Скопление жидкости в плевральной полости, известное как выпот, может возникать из-за множества заболеваний с различными причинами и методами лечения. Симптомы плеврального выпота редко встречаются в одиночку, чаще они сопровождаются другими признаками, которые пациент может не замечать. Опыт врача играет важную роль в своевременной диагностике. В нашей клинике работают высококвалифицированные специалисты с большим стажем, многие из которых являются ведущими экспертами в своих областях. Для определения причин выпота и подбора оптимальной терапии необходимо пройти обследование. В клинике НАКФФ доступны все необходимые диагностические процедуры, которые можно пройти быстро и в удобное время.
Диагностика гидроторакса
Процесс диагностики начинается с сбора анамнеза, в ходе которого врач исследует наличие хронических заболеваний, которые могут привести к скоплению жидкости в плевральной области.
При физикальном осмотре выявляются выбухание межреберных промежутков, ослабление или полное прекращение дыхательных движений грудной клетки. При аускультации слышно ослабление или отсутствие везикулярного дыхания.
Обязательно выполняется рентген грудной клетки в стоячем и лежачем положении. На снимках будет заметно равномерное затемнение, опускающееся в нижние отделы легких.
- Общий клинический анализ крови – для выявления признаков воспаления и анемии;
- Биохимический анализ крови – для оценки уровня белков, а Возможных проблем с печенью, почками и пищеварением;
- Тиреоидный профиль.
Пункция при гидротораксе выполняет две задачи: удаление скопившейся жидкости (лечебная) и лабораторное исследование полученного пунктата (диагностическая).
Полученную при пункции жидкость исследуют на наличие бактерий и атипичных (раковых) клеток. Проводится проба Ривальта для того, чтобы понять, какая именно жидкость скопилась: экссудат (воспалительная) или транссудат (образовавшаяся в результате нарушений белкового обмена или повышения гидростатического давления). При гидротораксе проба (реакция) Ривальта отрицательная.
Лечение гидроторакса
В основном лечение проводится консервативными методами. Для снижения давления в плевральной полости возможно выполнение пункции или дренирования – постоянного удаления жидкости. Этот метод не применяется только в случаях малозначительного гидроторакса, когда дыхательная функция остается относительно нормальной.
При любом хроническом заболевании, вызвавшем гидроторакс, рекомендовано лечебное питание – стол № 7 по Певзнеру. Ограничивается количество поваренной соли, белка животного происхождения и жидкости, добавляются сухофрукты для увеличения поступления калия.
- Для сердца – использование гликозидов, диуретиков (сохраняющих калий), сосудорасширяющих средств;
- Для печени – применение антибиотиков, принадлежащих к цефалоспориновой группе, и гепатопротекторов;
- Для почек – применение антикоагулянтов, гипотензивных средств и внутривенных вливаний альбумина;
- Для щитовидной железы – тиреоидные гормоны.
Прогноз при гидротораксе зависит от того, удастся ли компенсировать основное заболевание. Нарастание полиорганной недостаточности – плохой прогностический признак. Основная профилактика – постоянное врачебное наблюдение при хронических болезнях сердца, печени, почек, щитовидной железы, своевременное купирование обострений.
Методы диагностики

Заболеваниями легких и плевральной полости занимаются пульмонологи. Обычно пациенты обращаются к врачам по поводу прогрессирования симптомов дыхательной недостаточности при первичных заболеваниях. Во время приема врач выслушивает жалобы, изучает анамнестические данные для поиска причины симптоматики и проводит физическое обследование.
Часто уже на этом этапе обнаруживаются характерные признаки первичных патологий, включая отек брюшной полости и нижних конечностей. Во время перкуссии и аускультации легких также легко обнаруживаются признаки скопления жидкости в плевре. Для уточнения диагноза и необходимы данные дополнительных обследований.
Инструментальные и лабораторные исследования включают:
- Анализ крови для определения заболеваний печени, почек и других патологий, которые могут вызвать скопление жидкости в плевральной области.
- Электрокардиограмма – исследование электрической активности сердца для определения причин гидроторакса.
- Эхокардиография – ультразвуковое исследование сердца, в ходе которого могут быть выявлены признаки сердечной недостаточности.
- Рентгенография грудной клетки – для визуализации легких и плевральной полости с целью поиска патологий.
- Компьютерная или магнитно-резонансная томография – высокоточные методы диагностики органов грудной клетки. Это идеальный способ для выявления причины гидроторакса, где пульмонолог может обнаружить злокачественные новообразования или расстройства сердечной функции.
- Плевроцентез – забор серозной жидкости из плевры для лабораторного анализа и исключения плеврита. Процедура включает введение иглы между ребрами для извлечения небольшого объема жидкости. Пункция не только диагностирует, но и способствует облегчению состояния пациента.
- Эндоскопическое обследование грудной полости для раскрытия причин заболевания. При необходимости может быть взят образец плевры или легочной ткани для гистологического анализа с целью выявления раковых клеток.
Использование сразу нескольких методов диагностики важно для обнаружения первичной патологии и эффективного лечения.
Лечение
Лечение данной патологии не вызывает сложностей. Главной задачей является удаление избытка жидкости из плевральной полости для облегчения дыхания, а также коррекция основной причины заболевания. Удаление жидкости обычно осуществляется с помощью пункции, но в некоторых случаях может потребоваться открытая операция. После хирургического вмешательства врачи также устанавливают дренаж для удаления жидкости из плевры.
К сожалению, врачам не всегда удается устранить основное заболевание, провоцирующее скопление жидкости в плевре. При поздних стадиях цирроза печени и сердечной недостаточности единственным способом лечения может быть только трансплантация органов. Иначе дела обстоят с онкологическим источником заболевания, поскольку первичную опухоль можно удалить хирургическим путем.
Таким образом, гидроторакс, лечение которого иногда требует устранения патологических процессов других органов, является разновидностью плеврального выпота. Прогноз этой болезни условно благоприятный. При появлении первых признаков скопления жидкости в плевральной полости необходимо обратиться к врачу. Во время консультации пульмонолог объяснит тактику лечения и поможет выявить первопричину болезни.








